一种名为 lecanemab 的抗体药物,明显降低了临床试验参与者大脑中淀粉样蛋白斑块的数量,并减缓了他们的认知能力下降。在试验中,这项治疗使认知衰退减缓了 25%,足以让参与者多享受几个月的独立生活。 这给征服这种影响全球数千万人的破坏性疾病带来了希望。研究人员正在寻找药物组合、疫苗和基因疗法,以打造下一代治疗方法。
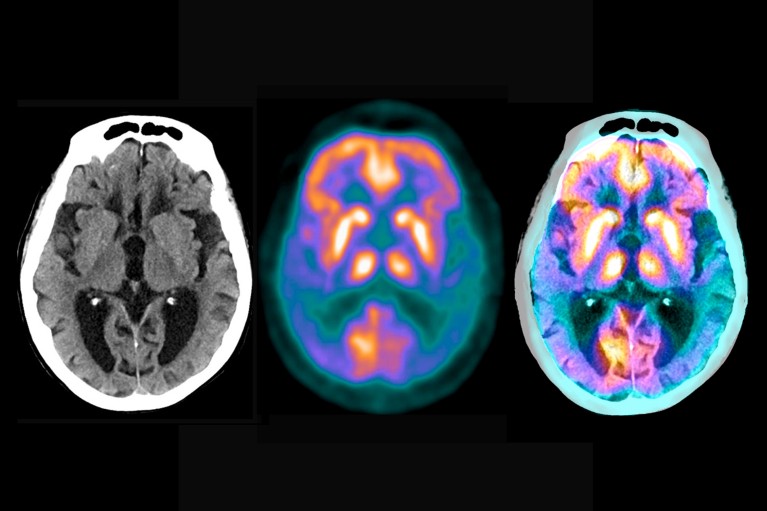
脑部扫描揭示了阿尔茨海默病造成的损害程度
去年 12 月,神经学家 Reisa Sperling 在一次国际阿尔茨海默氏症会议上接受了终身成就奖——在阿尔茨海默氏症(AD)治疗临床试验方面的突出工作而获奖。
她发明了一种名为 lecanemab 的抗体药物,明显降低了临床试验参与者大脑中淀粉样蛋白斑块的数量——该疾病的一个明显征象——并减缓了他们的认知能力下降。在试验中,这项治疗使认知衰退减缓了 25%,足以让参与者多享受几个月的独立生活。 这给征服这种影响全球数千万人的破坏性疾病带来了希望。
在获奖台上,斯珀林紧紧抓住麦克风,心情愉快。她在马萨诸塞州波士顿的哈佛医学院经营一个实验室,在阿尔茨海默氏症研究中已度过了漫长而令人沮丧的 30 多年,默默耕耘着,终于有证据表明她和她的同事走上了正确的道路。 “但是,这还不够,”她说。
尽管它还不完美,比如有严格的治疗方案,必须由专业护理人员通过静脉输注,而且药物可能会导致潜在的生命危险脑肿胀和出血,必须定期监测服用它的人等等。
尽管有这些瑕疵,但 lecanemab 的结果给人们带来了治愈的希望,即如果足够早地给予治疗,阿尔茨海默氏症最终可能是可以预防的。
这一成功也提出了另一种可能性:这种药物和未来的药物可以组合使用来应对疾病的不同阶段,这些阶段通常由不同的分子控制。很少有人期望单一疗法能够解决问题。但联合治疗试验既昂贵又复杂,因为每种药物都必须单独进行测试,并与其合作伙伴一起进行测试。制药公司可能会谨慎地将他们的产品与另一种产品捆绑在一起,以防组合失败并给他们的药物蒙上阴影。
该领域的信心增强不仅要归功于抗淀粉样蛋白抗体的成功。还有数不清的潜在药物,橱柜里已堆满了潜在的新疗法——以及现在正在清理的废弃药物。
有前途的组合
阿尔茨海默病的发病有一个漫长而无声的开始。首先,斑块——粘性β-淀粉样蛋白团块——开始聚集在大脑中。它们很快被称为小胶质细胞的免疫细胞包围,这些免疫细胞试图蚕食它们,但最终失败了。
斑块的大小和数量都在增长,但多年来甚至几十年都没有引起注意,直到它们导致另一种称为 tau 的蛋白质积累到有毒水平并以缠结的形式散布在大脑周围。阿尔茨海默病症状的严重程度就与 tau 蛋白缠结的范围相关。目前的证据表明 tau 蛋白是阿尔茨海默病症状、残疾和最终死亡的始作俑者。
迄今为止,针对 tau 的个体疗法在试验中表现不佳,但科学家们认为,与抗淀粉样蛋白疗法结合使用时,破坏 tau 蛋白的药物可能效果更好。
“我们知道淀粉样蛋白以某种方式驱动病理性 tau 蛋白的积累,然后它像野火一样在大脑中传播,”密苏里州圣路易斯华盛顿大学的神经学家贝特曼说。 “所以我们认为,在我们试图扑灭 tau 蛋白缠结之火的同时,去除助长火焰的物质是有意义的。”

贝特曼和他的同事将进行抗 tau 抗体和抗淀粉样蛋白抗体的试验
贝特曼和他的同事们在 2015 年开始计划进行这样的试验,但直到最近才变得可行,因为淀粉样蛋白疗法被证明有效。
去年,他们启动了一项名为 Tau NexGen 的国际试验。他们正在招募 168 名参与者,他们都可能在年轻时患上阿尔茨海默氏病——通常在 30 多岁、40 多岁或 50 多岁——因为他们的基因突变导致他们过度产生淀粉样蛋白-β。所有参与者都将接受 lecanemab 和 tau 还原抗体。
参加者是被分成两组,根据他们是否已经出现痴呆症症状或预计在未来十年内出现症状(这些人通常在与他们遗传突变的父母大约相同的年龄出现症状)。
所有参与者都将接受 lecanemab 和 tau 还原抗体,但顺序不同。那些没有症状的人将接受一年的抗 tau 抗体 E2814,然后添加 lecanemab;有症状的组将接受为期六个月的 lecanemab,然后添加 E2814。进行试验的研究人员希望他们可以使用这种设置来了解最佳治疗组合。
更多抗 tau 药物最终将被纳入研究,预计 2027 年之后将获得第一批试验结果。
Tau NexGen 是第一个,也是迄今为止唯一一个正在进行的联合治疗该病症的临床试验。一项类似的美国试验3正在计划用于散发性、迟发性阿尔茨海默病,该病影响老年人并占绝大多数病例。美国国立卫生研究院 (NIH) 预计将在未来几个月内决定是否将作为与制药公司的公私合作伙伴关系共同资助这项名为 ATP 试验的工作。如果是这样,招聘可能会在明年开始。
许多制药和生物技术公司正在开发抗 tau 疗法,一些作为抗体,另一些则使用其他小分子或更新的遗传方法来阻止病理形式的 tau 的产生。 ATP 试验的联合负责人、加州大学旧金山分校的神经学家 Adam Boxer 表示,其中几家公司已正式表示有兴趣参与。
与 Tau NexGen 一样,这将是一种预防试验。参与者几乎没有或根本没有可检测到的症状,但会从血液测试和扫描中获得证据,证明他们的大脑含有斑块和 tau 蛋白缠结的早期迹象。将有 6 组约 900 名参与者,他们将接受两种 tau 疗法中的一种,单独或与 lecanemab 联合使用,单独使用 lecanemab 或安慰剂。
研究团队希望抗 tau 治疗能够提高 lecanemab 的适度益处——并且在良性循环中,通过减少斑块负担,lecanemab 将为抗 tau 治疗创造更好的条件。
试验的关键是一系列敏感的新生物标志物——大脑或血液的测量,可以读出疾病状态。脑部扫描监测淀粉样斑块和 tau 蛋白缠结的存在和严重程度;血液或脑脊液测试可测量病理链中的许多其他分子,例如不同形式的淀粉样蛋白和 tau 蛋白。研究人员期望他们产生的大量分子和临床数据将有助于揭示更多关于阿尔茨海默氏症的机制。 “目前的证据表明 tau 是阿尔茨海默病症状、残疾和最终死亡的始作俑者,”Boxer 说。 “但这个假设需要在人类身上进行测试。”
联合疗法的试验有一些缺点:它们复杂且成本高昂。 抗体本身就是昂贵的治疗方法。 Lecanemab 一年治疗的售价为 26,500 美元。 Aducanumab(阿杜那单抗)一年治疗的原价为 56,000 美元,但在公众强烈抗议后,制造商将价格减半。
这些药物对患者来说也很不方便,因为它们必须每隔几周输注一次。临床试验的数据表明,需要终生治疗才能阻止阿尔茨海默氏症。 当输液停止时,这种疾病似乎会反弹。因为长期抗体治疗是不切实际的,他说,“我们认为,一旦抗体清除了斑块,用一种能阻止肽生成的口服药物来维持低淀粉样蛋白状态可能是有意义的”。
这样的化合物确实存在。从 2010 年左右开始,研究人员试用了一套口服药物,旨在通过降低两种酶(β-分泌酶和 γ-分泌酶)中的一种酶的活性来减少大脑中的淀粉样蛋白,而这两种酶是其产生的关键。但这些药物的临床试验都失败了4,对他们的兴趣枯竭了——直到他们得到第二次机会。
其他成分
2018 年,一群制药公司同意在他们通常保密的行业中做一些不寻常的事情。他们决定相互分享来自六项失败试验的机密临床数据,并与阿尔茨海默氏症协会召集的一组选定的专家分享,阿尔茨海默氏症协会是一个位于伊利诺伊州芝加哥的患者权利游说团体。
该协会希望从灾难性的临床试验中学到尽可能多的东西,每项试验都测试了一种不同的 β-分泌酶抑制剂。这些药物都没有显示出益处——更糟糕的是,许多药物都有毒副作用,包括在某些情况下认知能力恶化。该协会不想让试验数据在闭门造车中尘封,而是希望对它们进行详细讨论。该协会的首席科学官 Maria Carrillo 表示,目标是“帮助该领域更多地了解这些研究药物针对的疾病相关生物学”。
该小组于 2021 年发表的评论文章表明,对于此类药物而言,试验参与者的疾病可能已经发展得太晚,无法改善症状,并且较低的剂量可以避免副作用。
Aisen 认为应该有可能以低剂量使用这些药物来阻止斑块复发——一旦现有的斑块被抗体清除。
一批针对γ-分泌酶的临床试验也失败了。但研究人员并没有放弃这个目标,而是一直在研究一种更微妙的方法。他们没有完全阻断这种酶——一种导致试验中观察到的毒副作用的钝器——而是希望改变它的行为。
一种这样的调节剂,一种在学术合作中开发的化合物, 今年将在早期临床试验中进行测试。这种可以口服的药物会导致酶将淀粉样蛋白切成更短的蛋白质,这些蛋白质无毒,甚至可以起到保护作用。该试验将由一家位于马萨诸塞州波士顿的初创公司 Acta Pharmaceuticals 赞助,并由 NIH 资助。
考虑用于联合试验的大多数药物以淀粉样蛋白或 tau 蛋白为目标。但是这里有早期方法旨在改善大脑针对阿尔茨海默氏症的天然免疫防御机制。再一次,研究人员从具有使他们易患阿尔茨海默氏症的基因突变的家庭中学到了很多东西。
所讨论的突变发生在一个名为 TREM2 的基因中,该基因会产生一种位于大脑免疫系统战士小胶质细胞表面的分子。 “调整小胶质细胞可以使它们更有效地清除斑块或防止淀粉样蛋白病理学扩散,”德国慕尼黑路德维希马克西米利安大学的神经科学家 Christian Haass 说,“特别是如果斑块负荷首先通过抗淀粉样蛋白疗法减少的话。”他正计划在小鼠身上进行实验,以测试结合 TREM2 并激活小胶质细胞的抗体如果与抗淀粉样蛋白疗法一起服用,可能会如何发挥作用。一种类似的抗体作为单独治疗正在进行早期临床试验。
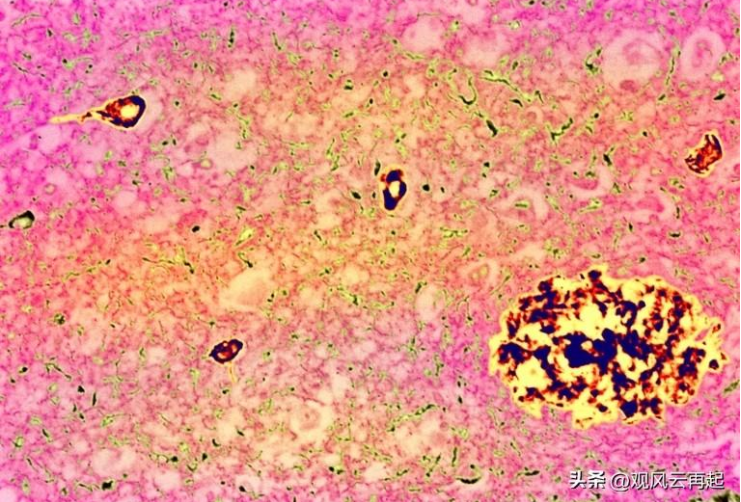
阿尔茨海默病的典型特征:斑块(大块)和 tau 蛋白缠结(小块)
疫苗、基因和血浆
更多阻止阿尔茨海默氏症的方法正在进入临床试验。研究人员的目标是通过疫苗、病毒载体或输血将有用的分子输送到大脑。
与酶药物一样,疫苗也在重新发明,这是在 2002 年第一次抗淀粉样蛋白疫苗临床试验停止,原因是当时在一些参与者中观察到了脑部炎症。
许多制药和生物技术公司正在开发更多的抗 tau 疗法,一些作为抗体,另一些则使用其他小分子或更新的遗传方法来阻止病理形式的 tau 的产生。
现在有几种抗 tau 和抗淀粉样蛋白疫苗正在准备或处于早期临床试验阶段。它们包含 tau 蛋白或淀粉样蛋白-β 的片段,经过选择和包装以避免严重的炎症反应。它们旨在刺激大脑的免疫系统识别和破坏蛋白质的完整版本,主要用于预防疾病或减缓早期疾病的进展。科学家们甚至正在尝试开发同时攻击 tau 和淀粉样蛋白-β 的疫苗。
其他研究人员正在押注基因疗法来征服由基因突变引起的阿尔茨海默氏症。但基因疗法并不适合所有人,因为已知的基因突变只决定了一小部分阿尔茨海默病病例。但替代疗法的概念已被其他人采用。位于加利福尼亚州圣卡洛斯的 Alkahest 公司已经完成了一项小型临床试验,测试年轻人血液中的因子是否可以替代衰老过程中丢失的因子。
现在说这些潜在的新疗法中哪一种(如果有的话)会成功还为时过早。大多数研究人员认为治疗需要个性化:处于不同疾病阶段的个体需要不同的疗法。 “很高兴看到有这么多可行的方法被采用,”艾森说。 “但我们还有很长的路要走。”
尽管如此,Sperling 说,通过临床测试的选择范围仍然令人鼓舞。“我们新的成功之光正在推动我们前进。”
文章来源于:健康界


 联系我们
联系我们
 返回
返回